テクノロジーとサイエンスの間
今回インタビューすることになった丹羽さんについては、記事の公開順が前後していますが、手作業の森田さんから「中高の同級生なんですが、何をしてるのか全然わからないので聞いてみてほしいです」と言われました。丹羽さんの所属は分子標的化学研究チーム。なにか化学的な研究なんだろうと思うものの、生物学が中心のBDRで一体どんなお仕事をされているのかやっぱり全然わからないということで、ネホリハホリ聞いてきました。(聞き手:薬師寺秀樹)
生物学に対して化学ができること
丹羽さんが所属している分子標的化学研究チーム、名前だけだとよく分わからないんですが、何を研究しているんですか?
身体の中の何かしらのタンパク質を見るための分子を作るというのが、チームのミッションですね。自分としては基本的に好きなのは化学なんですが、センターは生物学をメインとしているので、じゃあ化学が生物学に対してやれることってなんだろうと考えると、方法論とか分子ツールの開発みたいなことになるんですよね。
じゃあ、ツールを開発する人、みたいな立ち位置ってことですか?
センターで進めるサイエンスは完全に生物学側に重心がありますね。なので、そのための手段を開発しているというのが僕らの今の立ち位置です。
このセンターには生物学者さんがたくさんいるわけですけど、いろいろと話を聞くと、それなりに化学的に困っていることはあるみたいなんですよね。せっかく生物学者の近くにいて、生物学者との縁もできて、だったら化学の力で生物学を進めることができないかなというのは考えています。
生物学の人たちからすると、興味のある分子を追跡するためのプローブとかが欲しいのかな?
そうですね。分わかりやすいのでいうとプローブですね。もうちょっと頑張ると生体内の分子を生体内でプローブ化するとか、小さい分子で特定のタンパク質だけ標識してあげるとか。うまく展開できると、それらは診断や治療の方法にもなります。
でも、それだとものづくりというか、工学的なところで終わってしまうので。僕自身のサイエンスの興味はやっぱり化学にあるので、そういうプローブを作りながらも、新しい分子の設計方法なんかをきちんと考えるようにしています。
まだスパコンより脳
どうやって分子の設計をするんですか?
僕は学生のときからずっと新しい反応の開発というのをやってきているんです。5年に1回くらい化学でノーベル賞が出る分野で、本来くっつかないはずのものをカチャン!とくっつける方法論を開発するのが有機反応の開発なんです。
くっつかないものを、どうやってくっつけるんですか?
いろいろな手段があるんですけど、単純に言ってしまえば、大体の場合、プラスとマイナスがくっつくんです。別に新しいことをしなくても、ナトリウムイオン(Na+)と塩化物イオン(Cl–)を持ってきたらプラスとマイナスなので塩(NaCl)になるみたいな。有機化合物の中にも、細かく見るとこのへんがプラスっぽい、このへんがマイナスっぽいという電荷の分布の揺らぎがあるんです。そのプラスっぽいところとマイナスっぽいところをつなげるのが有機化学の最初のとっかかりになります。
それって小さな分子だったらなんとなくイメージが分かるんですけど、大きい分子になったときにはシミュレーションになるんですか?
シミュレーションですね。経験上、いっぱい教科書とか研究を見てきているので、分子の形を見たらだいたいここがプラスっぽくてこっちがマイナスっぽい感じかなー、みたいなイメージはありますけど、厳密な議論をしたかったら感覚では許されないのでちゃんとスパコンとか使って計算しますね。
じゃあ、今はシミュレーションでいろいろ設計できるんですね。
それがそうでもないんです。化学反応にはくっつき方に無数の可能性があります。エネルギー障壁の山を越えて谷に落ちて安定な構造に行き着くわけですが、そのルートは無数にあるんです。なのでスパコンでその計算をするのには莫大な計算時間がまずかかります。
さらに、AとBが直接くっついて反応してCができると思っていても、例えば実はA側が別のものと反応して、ぜんぜん違うDができて、DとBから反応してるみたいな可能性も考えないといけないんです。その全部を計算機上でやると終わらないんです。なので、ある程度人の頭の中で可能性を絞ってから計算を始めるということになります。
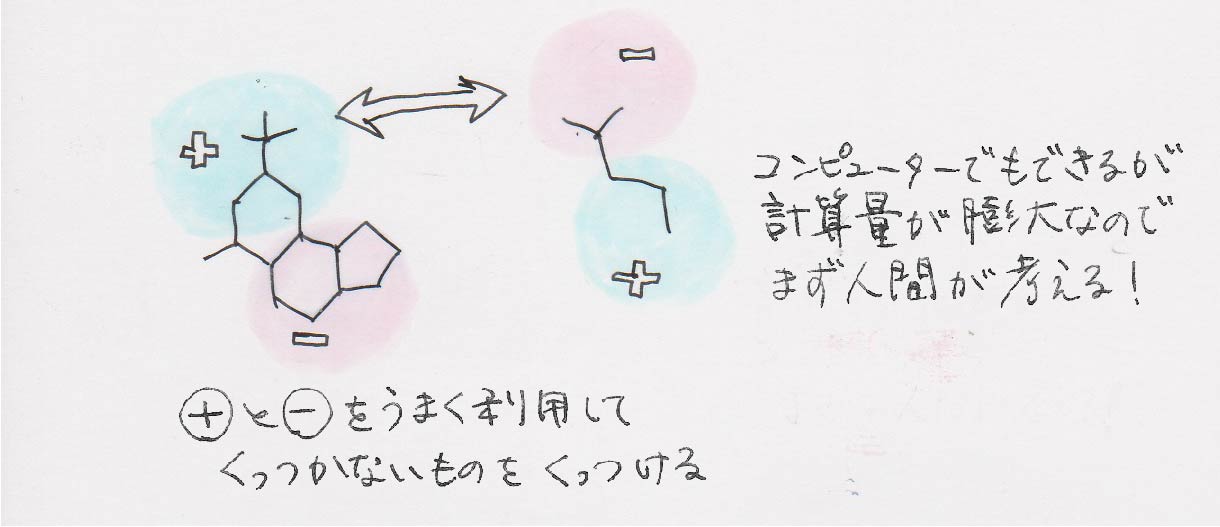
あれ分子の中の電子の部分の図みたいの見ることあるんですけど、あんな感じで設計しているんじゃないんですか?
あれは後付けなんです。きちんと反応が進んだときに、なんでその反応が起きたのかというのを解釈するために計算するんです。
そうなんだ……。
分子を簡単に変身させる
生物学側から「こんなの見たい」というリクエストがあったとして、どうやって進めるんですか?
元になる分子がある場合は、それをベースにします。PET(ペット)という病院のがん検診などで使われる装置があるんですが、その装置を使うとその目的の分子が体内のどこにあるのかということを追跡できるようになります。ただ、PETで追跡するためには、放射性同位体を元の分子に組み込む必要があります。
18F(フッ素の放射性同位体)とかですね。
そうそう、そういうのです。医薬品には結構このF(フッ素)が分子の安定化のために使われているので、普通(放射性ではない)のFを放射性のFに変えてやることができれば、効率が良いわけです。そこで、この変換を可能にしました。
もともとついてるFを外して、あらたにF*(放射性F)をつけるってこと?
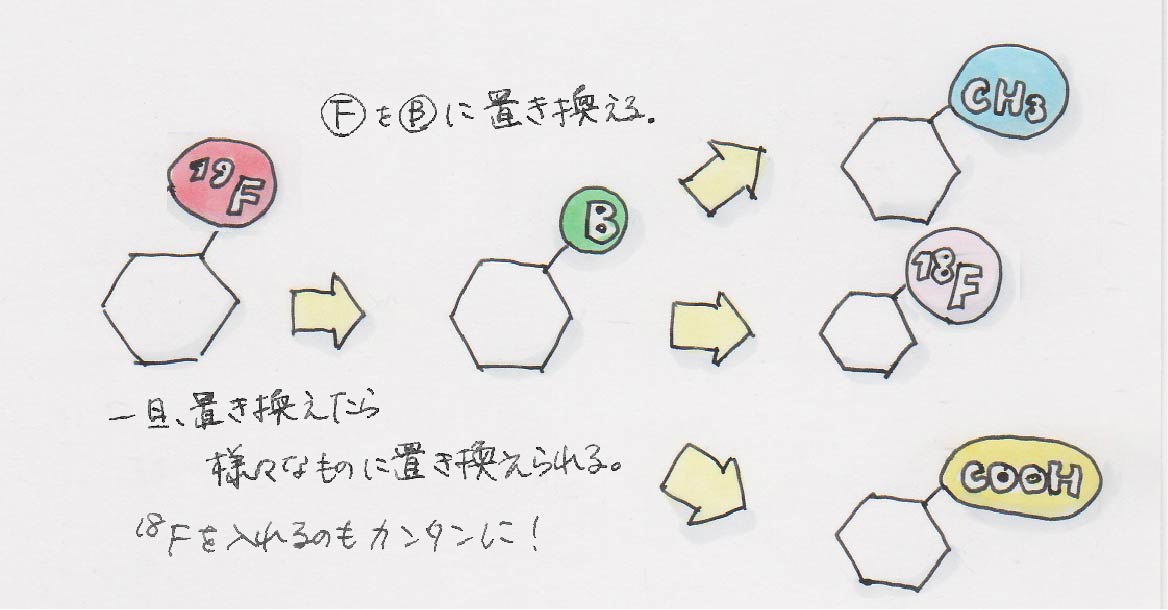
そうです。実際には一旦B(ホウ素)を使います。簡単にいうと、FをBにしてBをF*にする、という手順です。これがいいのは、最後のF*が他のものでもいいんです。Fを外すのはとても大変なんですが、Bはマイルドな条件で外れてくれるので便利なんです。そうするとひとつの元の構造からいろんな分子構造に展開することができるようになる。これを僕らは「分子リノベーション」と呼んでます。
失敗談も公開したらもっと進む
じゃあ、元の分子がない場合はどうしてるんですか?
実は、分子があっても、例えばフッ素を入れる場所がありませんとか、今の技術では炭素も入れることができませんみたいなのがあって、標識できない分子がまあまああります。
一方、元の分子がない時は、半年から1年待ってもらえるなら、みたいな話からスタートですね。それでも、反応経路が構築できないこともあって、やってはみたけどうまくいきませんでした、で終わることもあったりします。
ってことは、それは世の中に公表されることはないってことですね。
そういうケースだけじゃないですね。半年、1年かけて合成したプローブでも、きっちり結果が出るかどうかは生物に投与してみないと分からないわけです。動物に打った瞬間に代謝されて、何も見えませんでしたで終わる可能性も全然あるわけです。
なんか、「やった損」ですね。
生物は複雑ですから、しょうがないんですけどね。
だから、分子リノベーションの話は、これを効率化できるんじゃないか、という発想で始めたものでもありました。
「できなかった」情報が失われるってのは、もったいないですね。
大体うまくいってない例って世の中に出ないんですよね。これが問題で。やってる本人がつらいのもありますけど、駄目な例ってやっぱ知っておきたいんですよね。そういう駄目なデータを集めようジャーナルみたいなのありますよね。
これ駄目なんだというのが、調べて分わかればずいぶん早くなるんだろうね、きっと。
そういう状況であれば、自分が考えたことは大体誰かがやっているという体でやるので、1回パッと検索して、こいつやってんだで、その条件を細かく見てとかやれたらだいぶ効率化できますよね。
駄目だったほうもそうですけど、うまくいったほうについても評価が難しいところはあります。
有機合成って職人芸ってよく呼ばれていて、卒論生と修士課程と博士課程で明らかに技術が伸びるんですけど、合成力が。
職人の世界と微量な不純物……
同じ反応をやらせてみると全然収量が違うとか?
本当にそうなんですよ。こいつがやるとうまくいくけど、こいつがやるとうまくいかないとか、普通にあるんですよ。なぜかというと、実験項をいくら細かく書いても、ノウハウを書ききれていないんですよね。
ちょっとした試験管の揺らし方とか?
本当にそんな感じです。試薬の入れるスピードであったりとか、精製時の使う溶媒の量、水の量とか、分取のカラムとかを使うのに精製の方法であったりとか、ガラッと変わりますよね、人によって感覚が。ラボによっても違いますね。
今回、例えばさっきのFを外すホウ素化反応も、論文を出した後にメールが来て「うちのじゃいかない、何が違うんだ」という問い合わせが来ますし。
再現できないんだ。化学の反応の話でそんなことがあるんだ……。
自分がやっている反応が再現できないのは怖いので、僕はすぐうちの他のメンバーに再現できるかやってもらって、少なくともうちではできるということは確認しています。他所でもできるところもあるんですけど、できないところもやっぱりあって。その差って、入れ物のサイズであったりとか、加熱の容器であったりとか、使っている試薬の純度であったりとか、いろいろな要素が出てくるので、現地に行かないと分わからないですね。
純度って、試薬の?そういえば、以前試薬会社に勤めてた時に製造ロットが変わると、反応が進まないとかクレームが来てたりしてました。
あるでしょうね。僕らも、この化合物はいつもこのメーカーのを使うというのがあります。怖くて変えたくないという感覚です。
2000年代に起きたけっこう有名な話がありまして。触媒に使われる金属って高価なんですが、それの代わりに鉄が使えますよという論文が連発して出たころがあるんです。その後数年してから、純度の高い鉄だと反応がいかないということが分かったという論文が出て、逆に。結局、鉄の中にppmオーダーで入っていた銅が触媒活性種だったんです。
ppmというと、鉄の純度は99.9999%か。0.0001%以下の銅が反応していたんだ・・・!
僕らのケースでも似たようなすごいのありました。ホウ素を放射性の炭素11を持つシアノ基に変換する反応なんですけど、どうやっても期待通りの放射能が得られなかったんです。どうも放射性ではない普通の炭素12Cのメタンガスが混入しているのではないかと。でも、放射能を扱うときはホットセルと呼ばれる閉鎖された反応器で合成するので、外から12Cのメタンガスが混入することはまずあり得ない。
じゃあ何の純度が悪いのか?ということでやり玉に上がったのがアンモニアガスでした。11Cのシアノ基の原料の調製に使うものですが、この純度が99.999%。悪い数字ではないですが、12Cのメタンガスがわずかに混入しているかもしれない。そこで99.99999%の「超高純度」ものに変えたら解決。そんなこともあります。
話すと簡単に聞こえるかもしれないですけど、99.999%でもすでに「高純度」なのでなかなかそこに絞り切るのは大変でした。
実はなにが起きているかよく分からない
なんか化学ってもっとスマートなイメージがあったけど、結構いろいろあるんですねぇ。
ありますよ〜。
分子リノベーションの話にしても、実は「反応はうまくいったけど、なんでうまく行ったのかよく分わからない」というのが本当のとこです。電子分布の図が後付けと最初に言いましたけど、実は狙った反応経路とは違うようなんです。
あ、そうなんだ。
反応を開発するうちはまだ、サイエンスというよりは、工学なんですよね。「なぜうまくいくのか」の先がサイエンスなんですよね。どっちも重要で、どっちも楽しいんですけど、なかなかサイエンスに持っていききれないものも手元にはありますよね。
例えば、ある反応でニッケルを使おうと思うには、これまでの経験値とか、論文上のデータとかがあって使っているわけで、浅いサイエンスは無数にあるんですけどね。それを言語化できにくいところとかがあって、定量評価ができていないので、職人芸っぽくなるんです。「なんでこれ、ニッケルと銅を混ぜたの?」と「職人の勘みたいですね」みたいに言われたこともあったりしますし。
なんでその反応が進んでいるか?の解明みたいな感じになるわけですかね。
そうですね。ものづくり的には、フッ素がホウ素に置き換えられました、という話で全然いいんですけど、サイエンスとしてはまだ未達ですよね。それでも立派な論文にはなるんですけどね。
でも今後も生物学に関わるだろうから、いろいろ開発していくんですよね。
そうですね。生物学の研究と縁ができてしまったので、PETに限定はしないですけれど、生命科学の研究に役に立つ変換をもう少し考えていってあげられたらなとは思います。でも、これを言っているとまたサイエンスというよりは工学なんですよね。
じゃあサイエンスはなんなんでしょうね(笑)。

編集後記
再現性がなかなか取れないという話は生物学ではよく聞く話なんだけど、化学でもあるんだなぁ。フラスコの振り方だったり、試薬の入れ方など細かいところで合成効率が変わったりするという、結構ものづくりな側面をお聞きし、目からウロコでした。純度が99.999%じゃダメで、99.99999%だとOKとか、なんとシビアなことよ……。
