肺の研究は洞窟探検
今回ネホリハホリするのは森本充さん。肺の研究者!ということでおなじみですが、そもそもなんで肺なんだろう。肺のなにが面白いんだろう。そんなところから聞いてきました。(聞き手:薬師寺秀樹)
生物愛好会作ってみた
研究の対象は肺ですけど、肺を選んだ理由は何ですか?
僕は肺の発生と再生を研究しています。この分野は意外と国内では研究している人が少なく、世界的にも今まさに研究が進んできて、学問として体系的なものが作られつつある分野なんです。この分野を選んだ理由は、もともと内蔵の発生と再生に興味があって、この二つを繋げて考えられるような対象として、ポスドク時代にたどり着いたのが肺でした。
なるほど。その辺の経緯をお聞きできますか?
中学、高校では生物の授業が好きで、特に高校のとき生物部っていうのをやっていたんです。
とはいえ実は始めたときは、生物部というのはなかったんです。
え、ということは生物部を作った、ということ?すごいですね。
そうなんです。学校のルールで「愛好会」から始めないといけなかったんですけどね。生物の先生と仲良くて、「昔、生物部があったんだけど、なくなっちゃったんだよね〜。」という話を聞いて気になっていたし、生物調査のフィールドワークに憧れがあって始めました。
まぁみんなで集まってワイワイやること自体が楽しかったんですけどね。
なるほど、もともと生き物好きなんですね。
それで生命科学の世界に入っていくんですが、学位を取った時には細胞周期細胞は分裂する時に染色体のコピーが作られ、それぞれ反対方向に移動し、二つの細胞に別れるという状態を周期的に繰り返す。これを細胞周期という。セルサイクルともいう。の研究をしていたんです。細胞周期のプロセスに異常なことが起こるとガンになったり、細胞分裂が止まったりします。その細胞周期の進行を酵素の反応として理解するということが当時の主流で、僕が大学院生のときにノーベル賞が出た分野でした。トピックだったのがタンパク質の分解に関わるユビキチンープロテアソームパスウェイ経路。生体のさまざま現象は分子と分子の相互作用の連続。分子Aが分子Bと反応して、分子Cができて、分子Cが分子Dと反応して……、と繋がっていく経路のこと。というタンパク質を壊す細胞内の仕組みなんですけど、これが細胞周期にとても大事で、この分野に僕が学位を取った次の年にノーベル賞が与えられています。
世界的に流行ってた分野ですから、これはこれで面白かったんですけど、生物や生物を取り巻く環境が好きという元々の思いもあって「どうもこのテーマは生き物らしくないな」、「生き物を丸々理解する学問をやりたいな」と思い始めました。
体節形成は“大切”
学位を取った頃、ノックアウトマウス特定の遺伝子が機能できないようにした遺伝子改変マウスのこと。Knock-out。他にもKnock-downなどもある。が世の中で使われるようになってきた時期だったので、マウスの遺伝子組換え技術が学べるところを探しました。日本ではそれができる研究室は少なかったんですが、探した結果、遺伝研(静岡県三島市にある国立遺伝学研究所)の相賀裕美子先生の研究室でポスドクを募集していることを知り、応募して、雇ってもらうことができました。
そこで始めたのが「体節形成」の研究でした。これがすごく面白かったんですよ。体節形成とは、背骨の元になる胚組織のパターン形成のことで、脊椎に沿った尻尾の先までの縦方向の繰り返し構造を決めています。肋骨の繰り返しも体節の配列を反映しています。体に張り巡らされた神経も体節の構造に沿って広がっていくし、ほとんどの筋肉はこの体節の中から作られて、そのあと歩いて体に広がっていくんです。
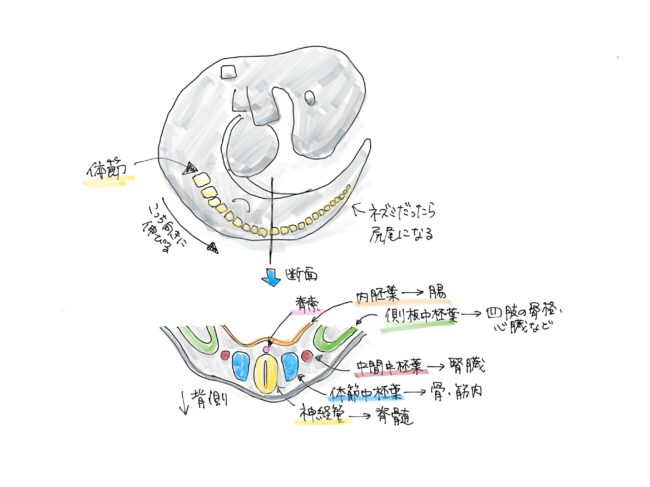
歩いてくる……?
筋肉って歩いてくるんですよ。
はじめに胎児の中胚葉という組織の一番お尻側に細胞の塊ができるんですけど、そのさらに先端部分が増殖をしながらニューっと伸びます。その後に筋が入って、プチッと切れる。で、これを繰り返して、結果、ボールが並んだような状態になります。
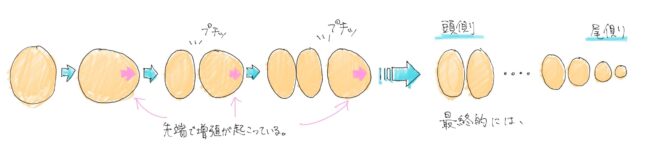
この一個一個のボールの中に、皮膚、筋肉、腱、軟骨のモトがあります。次にそれぞれの体節から左右に細胞が移動して広がっていくのですが、そのような細胞の中に筋肉の細胞もいます。また、胸の位置だったら肋骨のモトになる軟骨細胞もいます。神経は由来が異なりますが、この軸に沿って移動して伸びていくんです。なので、「歩いてくる」という言い方をしてます。
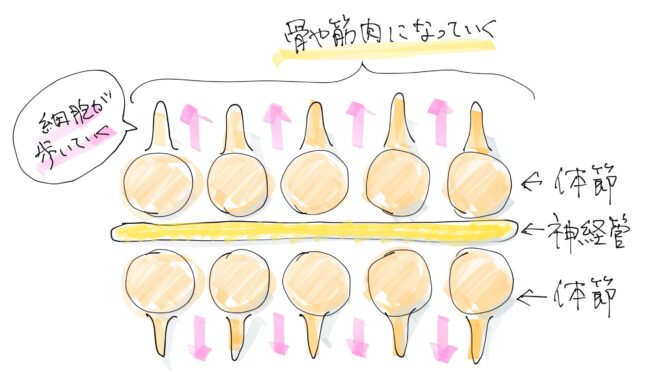
なるほど。体節形成は”大切”ですね(ドヤ)。
それ、学会のお約束です(笑)。
ちなみに、キリンの首の骨の数とヒトの首の骨の数は一緒なんですけど、これは元々の体節の持つ情報が共通しているからなんです。ところが、鳥は違う。鳥は首の骨の数が多いんですよ。これは体節が持つ空間情報の違いから来ていて、体節のどこから何を作るか、という情報が違うのでそういうことが起こるんですね。それは、大元の縦方向の空間情報の実体化とも言えます。
(ムズカシイお……)
分子でできた時計
体節形成を説明する理論はいろいろありますが、僕がハマってたのは、時計メカニズムです。頭側から体節ができていく際に、マウスでは2時間に1回切れるというのがわかっています。これが時計のように正確なので、時間を刻む時計メカニズムがあるんじゃないか、と言われていました。僕らの学生、ポスドク時代にこの時計に関わる分子が次々と明らかになり、国内では相賀研と京都大学の影山先生らが熱心に取り組んでおられた。
時計ですかー。どうやって時間を刻んでるんですか?
基本的には転写因子とその下流因子にネガティブフィードバックの関係があって、上流と下流で制御しあいます。そうすると、それぞれの濃度が上がったり下がったりを周期的に繰り返すことになるので、この遺伝子発現の波が時間を刻みます。
うさぎときつねの話みたいですね。
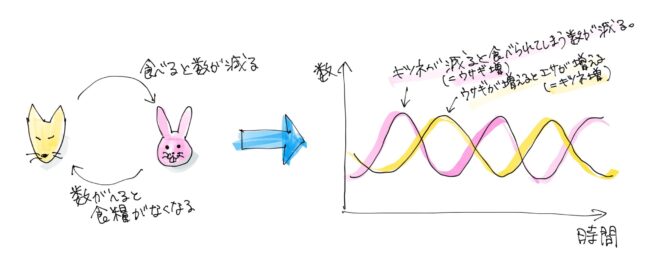
そうですね。そういうネガティブフィードバックはいろんなところにありますね。そういうのが発生学の分野でも証明されてきた時代でもありました。
僕らはそのオシレーション(振動)が、どうして「切れる」ということに結びつくのかというところを解こうとしていました。以前に、相賀先生がMesp2という体節形成のクリティカルファクターになる遺伝子を単離していました。これが現れると振動が止まるんです。ピタッと。そうすると一個の体節の大きさが決まって切れる。ちょうど1つの周期の幅で1つの体節の大きさが決まり、特に体節のMesp2が発現する部位の後ろで「切れる」ことを突き止めました。
さらに僕らは、どうしてこのMesp2が「切れる」場所を決められるのかということを特定したいと思って、ライブイメージングと遺伝学を駆使して、Mesp2の濃度が上がり将来的に切れる面の反対側にいる分子とのコントラストが高まったときに体節が切れることを証明しました。この仕事がNatureに掲載されて、自分のキャリアの中で大きなブレークスルーになりました。
おお。Nature科学雑誌の最高峰の一つ。他にScienceが有名。分野によって他にもあり、生物系だとCell、医学系だとNew England Journal of Medicine(単にNew Englandとも)などがある。他の研究者が参考にすることが多いため、業績としてはポイントが高い。!
それ以来、カタチという「目に見えるもの」を分子という「目では見えないもの」で説明できる、ということが面白くて、発生学にのめり込むようになりました。
そして肺へ……
研究対象としては以前から内臓をやりたいと思っていましたが、その当時は内臓の発生ってとても知識が古かったんですよ。
へー、そうなんですね。
当時は分子レベルの現象は教科書には載っていなくて、レビュー(総説)いろんな研究を整理して分野の動向やキーポイントなどを解説してくれるタイプの論文。新しい分野に取り組む場合など、はじめにメタ情報を掻き集めたいときに便利。とか、ざっくりとしたものがある状態でした。それで、内臓の研究ができるところはないかと探すなかで、アメリカのRaphael Kopanという人がいいということで、連絡をとりました。
そうしたら意外とあっさり「自分で研究費取って来ればいいよ」ということで、彼のいるWashington university in St.Louis(セントルイス)に行くことに決めました。そんなに都会ではないんですけど、研究にはとてもいいところでした。
知ってますよ、セントルイス。川の上にカジノがあるんですよね。
よく知ってますね。
これが当時の写真です。

おお。若いですね。森本さん、ずいぶんとガッシリしてる……
山登りばっかりしてましたからね〜(笑)。
研究対象としてはいくつか可能性があったんですが、せっかくやるなら新しいことをやろうということになって、肺が議論に上がりました。
内蔵の再生にも興味があると言ってましたが、再生する臓器と言えば肝臓だと思うんですけど、肝臓じゃなくて?
そうなんです。肝臓でもなく、腸でもなく、肺にしました。もちろん肺は本当に適切なのか、といろいろ調べましたよ。肺の論文はそんなに多くはなかったんですけど、思いがけず損傷再生の論文が多く見つかりました。そういうことができる実験系としてあるのだったら、もしかしたら肺だったら発生と再生を繋ぐような研究ができるんじゃないか?ということで、肺の研究に取り組み始めました。
ようやく肺にたどり着きましたね。
はい、ようやくです。
でも、肺の発生研究をしている人がそんなに多くはなかったので、情報収拾とか仲間づくりとかは本当に苦労しましたね。あと、呼吸器の発生にしろ再生にしろとにかく日本語では勉強できなかったんですよね。なので、せっかくアメリカにもいることだし、英語の文献だといくつかはあったので、現地で読み漁って一から勉強しました。
研究室としても新しい取り組みだったのでラボの中で教えてくれる人はいなかったけど、同じ大学の他の研究室にやってる人はいたので、その人のところに行って技術的なことを教えてもらったりしてました。
それで研究室の中に遺伝子改変マウスのリソースはいろいろあったので、そういうのを使ってNotchシグナリングと肺の発生を始めました。
なかなか大変ですね……。
でも、やりたい方向性がはっきりしていたのがよかったんだと思うんですけど、発生の時にNotchシグナルが活性化する細胞と再生の時に活性化する細胞が同じだというデータが1年くらいで得られました。
証明するには時間がかかりましたが、「やはり発生を再生は繋げて考えることができる」という確信を得ました。で、「よし。これで行こう。」と自分の中で固まりました。
発生と再生を繋げて理解する
発生と再生を繋げようと思ったのはなぜですか?
発生と再生が似てる、と言う研究者は結構います。
組織幹細胞は未分化の細胞ですよね。そこから機能的な細胞が現れるときは、またパターニングという機能細胞の配置が起こっている。再生は発生と同様にモルフォジェネシス(形態形成)が再現されているんじゃないか、と考えている人もいます。発生と再生が似てると言われているが実体はない、という状態だったと思います。
実体がないってどういう意味ですか?
分子レベルで説明ができない、ということです。
言い換えると、発生の時のこのキーの遺伝子が効いていて再生の時の同じ遺伝子が効いて同じプロセスだ、というような証拠がないということです。
発生は非常に少ない均一なものから、多くの異なる機能的な失態を作るプロセスです。一方で、再生というのは失ったものを取り返すプロセスで、部分的に何かが現れて周りと同じようなものに戻っていく現象です。そう考えると根底が違うわけだから、理論的に考えれば違って当然とも考えられます。でもやっぱり似てるという部分が見つかった時に、それをちゃんと体系的に説明できるものがあったらいいんじゃないか、ということを考えています。
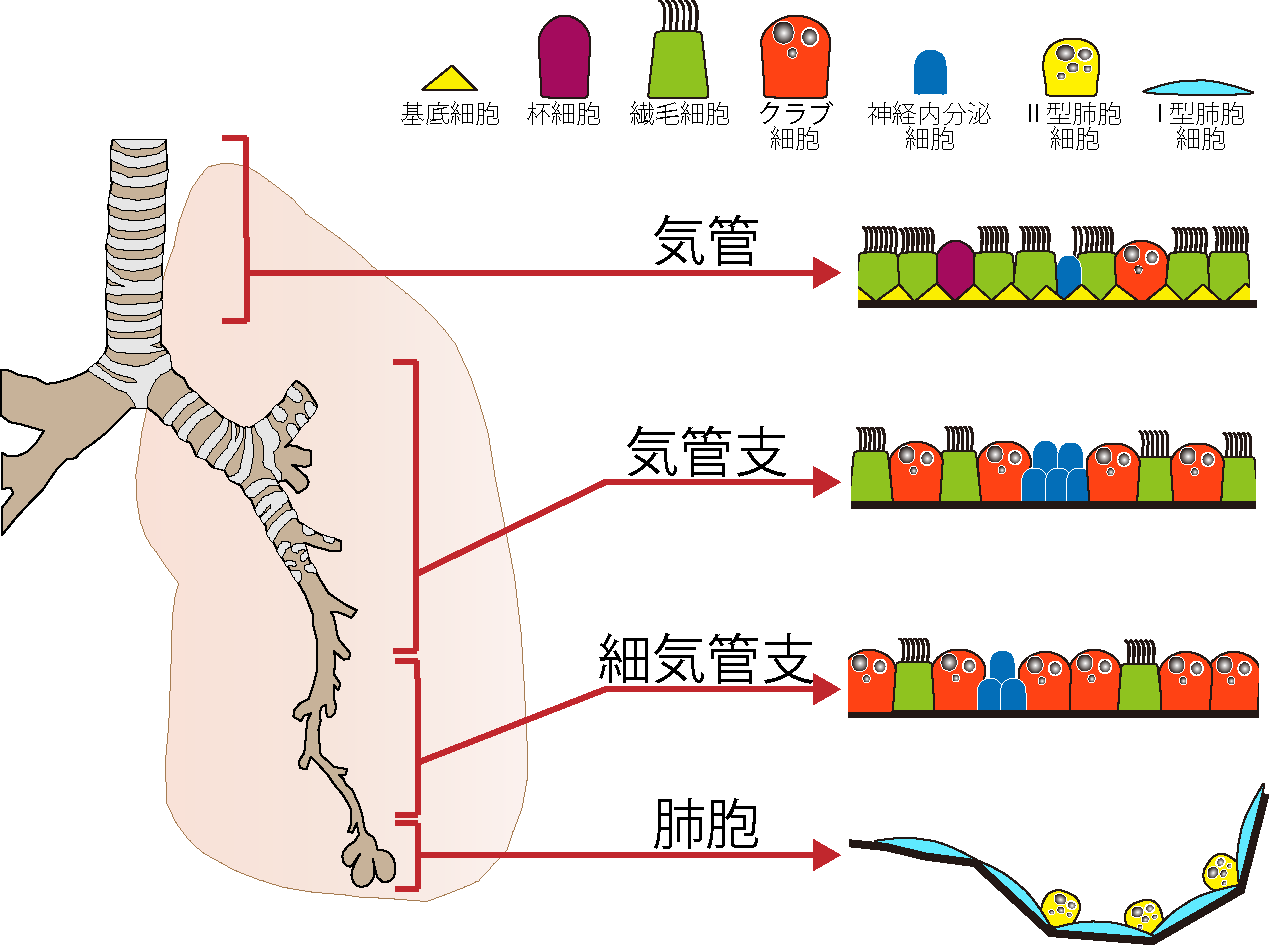
発生と再生が繋がるという方向で、一番初めに見つけたのは気管支のクラブ細胞でNotchシグナルが活性化しているということでした。
気管支の内側、上皮組織にクラブ細胞と線毛細胞という細胞が隣り合っているんですけど、クラブ細胞でNotchが活性化していて、隣の線毛細胞でNotchシグナルを活性化するリガンドがいることがわかりました。つまり、この二つの細胞の関係性は、与える側と受ける側の関係なんです。
実態としての分子
Notchシグナルは、ごく短距離の細胞間で起こる情報伝達ですけど、作用する側も作用される側も分子としては膜貫通タンパクだというのが特徴です。つまり、隣り合う細胞でしか起こらない相互作用だということです。
ちなみに数年前に、Notchシグナルが活性化するプロセスのアニメーションを作ったんですよ。
え?作った?
友人と二人で作りました。彼も研究者です。
ほんとだ、Scientific Directorって書いてある。
この相互作用は物理的に引っ張るってのが特徴なんですよ。そうするとレセプター(受容体)の構造が変わって、プロテアーゼタンパク質分解酵素。〇〇アーゼというのは〇〇分解酵素だと思えばよい。「アーゼはドイツ語読みで、最近は英語読みの「エース」ということも多い。たとえば、プロテアーゼ=プロテエース。が寄って来て、切断する。切断されると細胞内ドメインが核の中に入っていってターゲットの遺伝子を活性化させる、という仕組みです。
なるほど。それがさっきの動画で再現されているんですね。
発生と再生が繋がっている
さて、登場人物の話を一通りしたので、話を戻しますね。
再生の話からすると、まず、Notchが活性化するとその細胞が青くなるという遺伝子改変をしたネズミを使いました。何もしない状態だと、クラブ細胞が圧倒的に青くなってほかの細胞だと全く青くならない。つまり、Notchは選択的にクラブ細胞で活性化していると言えます。
そこで、このマウスに薬剤を使って傷を負わせて時間経過を追って回復を見ていく、という実験をしました。そうすると初めは上皮が死んじゃってペラペラになります。そのあと残っている細胞が増殖して上皮がカバーされていくんですが、数日くらいで青い細胞が復活してくるんです。
死んだはずのNotchが活性化した細胞が復活するということですか。
そうです。再生現象の時には、Notch活性ではない組織幹細胞自体の中からクラブ細胞になっていくという方向の中でNotchシグナルが必要だ、ということが証明できました。
次に発生の話ですが、今度はKO(ノックアウト)マウスを使って、再生のプロセスでもクラブ細胞に依存してるっていうことを証明しました。
そうすると、発生の時にはNotchが活性化してクラブ細胞になっていくんですけど、再生の時にもこのプロセスが効いているということが言える。つまり、発生と再生で同じようなプロセスを共有しているということが言えます。
お。発生と再生が繋がってきた?
そうですね。いずれもNotchシグナルが共通してキーになっている、ということが言えます。なので、発生と再生はリンクしている、と言えそうです。
疾患にも関係している
実はこのプロセスは、喘息にも関係していることも発見されました。喘息がひどくなると過剰粘液症という症状が現れます。その原因の一つが粘液細胞の過剰な出現なのですが、これはNotchの過剰な活性化のせいなんです。ということは、本当に根幹的な生命現象は、ライフステージのいろんなところで共通しているということが言えそうです。
今後も幹細胞と上皮のパターン形成を通して、発生ー再生ー疾患の関係を探っていきたいと考えています。
理研に来てからは、ライブイメージングで肺の形成プロセスを観察することに力を入れています。というのも、従来の臓器を薄く切って観察するという手法だと、空間情報や時間情報が落ちていくんですよ。ライブイメージングだと時間と空間の情報を持ってデータを得ることができるので、情報量が断然多いし、なにより生きている様子が見えます。
これを使って、他の発生現象も追っています。たとえば、肺がんの一種に小細胞肺がんという転移が早いがんがあります。気管支の神経内分泌細胞という細胞が小細胞肺がんの起源の一つになるということはわかっていたんですけど、私たちの研究結果からこの細胞はもともと歩ける細胞で、がん化すると歩く能力が災いして転移が早いのではないかと考えていたんです。でもその証拠はなかった。実際にライブイメージングで見てやってこの細胞がどこで生まれ、どこに行くのかを見てみたんです。分岐点にいるということはわかっていたんですけど、実はもう少し根元のところで生まれて分岐点に歩いてやってくる、ということがわかってきました。
なので、転移が早いのはこの細胞がもともと歩くことができるからじゃないか?ということが想像できます。そうすると胎児の神経内分泌細胞を調べることで、小細胞がんへの新しいアプローチが見つかるかもしれないと期待しています。
細胞がつくるカタチ・パターン
さらに、このNotchなんですけど、細胞のパターニング(規則的な配置)にも効いています。正常だと線毛細胞の中に緑のクラブ細胞がごま塩を降ったように“まだら”になるんだけど、Notchがないと線毛細胞だらけになっちゃうんです。まず、Notchがないとクラブ細胞がいなくなって、線毛細胞が増えるんです。
で、どうしてそうなるかを調べると、どうやら発生のある特定の時期に決まっているのがわかってきた。
この時期は、最初は非常にシンプルな二股の気管支が、伸びながら分岐を繰り返して肺の構造を作っていくという段階です。この時にどうやってこの構造ができてくるかってことなんですけど、管の前端部分で細胞増殖が起こっていて伸びていくのが、根元では増殖が抑えられているということがわかりました。ちょうど植物の根っこのように。
先端部分は幹細胞が維持されて増殖しているんだけど、根元の方は比較的増殖は抑えられていて分化の方にいくんです。つまり、先端は幹細胞の塊なんですが、根元の方は分化細胞が増えていって、これによってチューブが伸びていく。なにやら、体節の話にも似てますよね。
幹細胞を特異的に染色する方法があるので、どこに幹細胞がいるかというのはわかります。そうすると、幹細胞は先端にいるはずなので、先端だけが染まるかと思いきや、根元の方も染まるんです。これは、根元の細胞が元は先端だったということの証明でもあります。
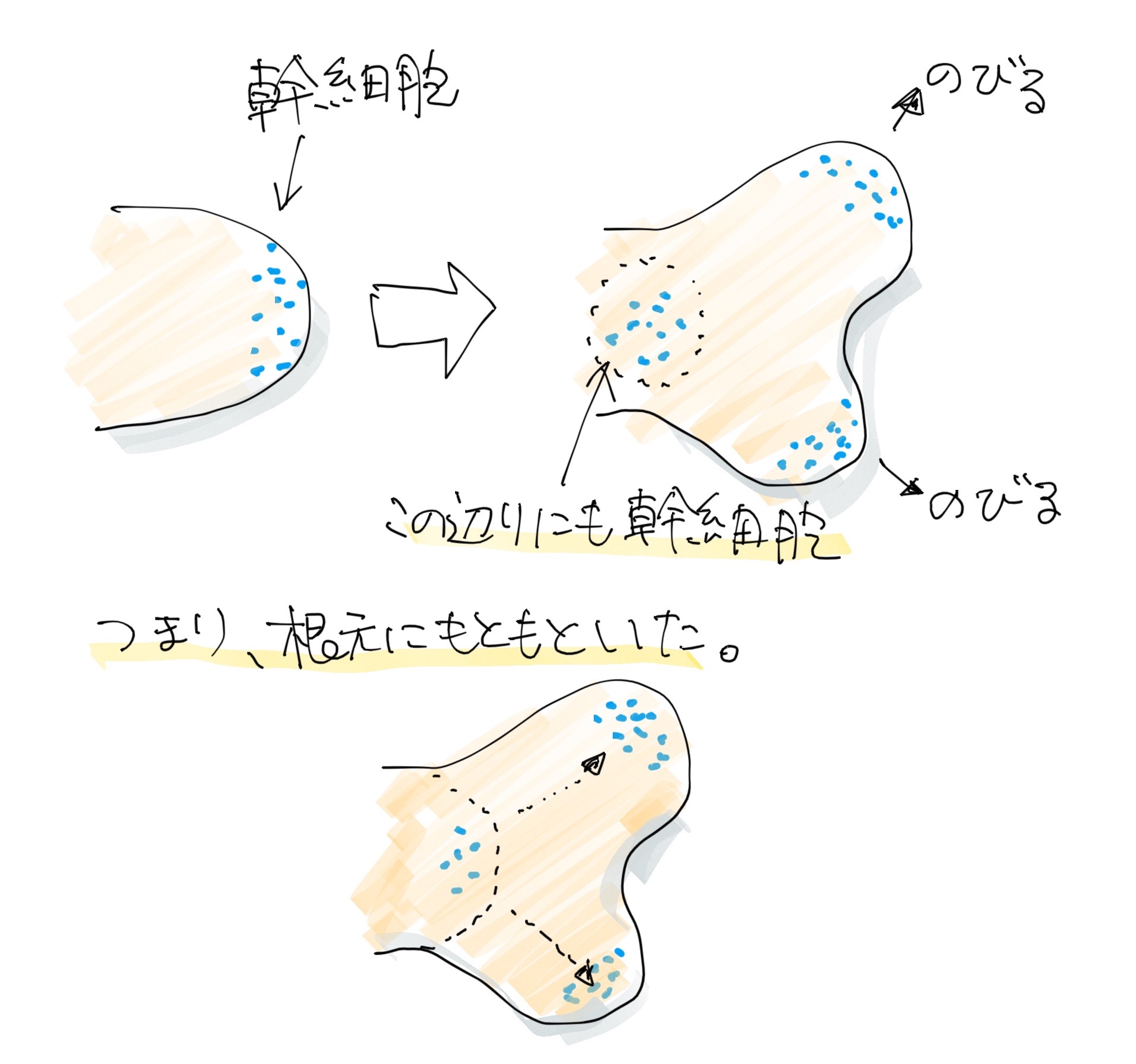
現在の僕らの興味は、幹細胞から分化した機能細胞が生まれる間の部分(Transition Zone)です。ここではクラブ細胞と線毛細胞のバランスがおかしくなっています。これにNotchが関わっているだろうと考えていて、これを証明したいと考えています。
ところで、伸びてくのはわかるんですけど、なんで分かれるんですか?
あ、それはいい質問。
今でも完全に証明はされていないんだけど、いくつか理屈があって、伸びるという現象は多少早くなったり遅くなったりしてるんじゃないか、という話があるんです。遅くなった後、次に伸びる時にまっすぐ伸びるんじゃなくて、一定の少し広がりながら伸びていくんじゃないか、とその時に真ん中にくぼみができて別れるんじゃないか、という理論があるんです。
体節のときの時計の話に似てますね。でも物理的にはどういう力がかかってるんですかね?
たぶん、ネガティブフィードバックがかかっていてオシレーションがあるのかもしれません。そこに平滑筋が入ってきて引っ張るということも言われていますが、実はまだよくわかっていません。
肺の研究は洞窟探検?
今はオルガノイド臓器もどき。Organ(器官)とoid(もどき)からできた造語。多くの場合は平面的に培養される細胞を、立体的に培養することで実際の器官の構造や機能の一部を再現することができるようになってきている。を使っていると思うんですけど、どういう経緯で取り組み始めたんですか?
実は、肺胞の幹細胞を培養するにはオルガノイドでやるしかなかったんですよ。なので、必然的にオルガノイドを使うようになりました。今はES細胞やiPS細胞を使って気管の3次元構造をオルガノイドからで作れないか、ということにもトライしています。
なんですが、これがなかなか大変で(苦笑)。気管はヘテロな細胞集団でできていて、内胚葉と中胚葉の両方が必要です。また大きく成長させるには血管を通してやらないといけないのですが、これがまたハードルが高い。
いろいろ同時に培養してやらないといけないですもんね。今後、他の臓器に展開したりするんですか?
以前はそんな風にも思っていました。ところが一旦肺に入り込んでしまうと奥が深くて。まるで洞窟探検です。
確かに、洞窟っぽい。
実は、洞窟探検もやってたんですよ。
Σ(・□・;)?
面白いですよ。洞窟探検。
(いや、そういうことじゃなくて……)

日本でも未探検の洞窟というのが結構ありますよ。学生時代に、沖縄の新洞窟探査にハマってました。自分でリーダーをやっていたこともあります。日本各地の洞窟、奥多摩行ったり、岡山に行ったり、結構いろんな洞窟に行きました。未踏だったら測量、作図もします。秋芳洞とかテレビ番組を見ていると昔の仲間が今もやっていたりします。
沖縄で入った時に、鍾乳石が上から迫って、鼻だけ水面に出して泳いで行かないと通れないところが何箇所かあってそれは大変でしたけど。ただ、それを超えると途端に綺麗な景色が広がるんですよ!壮観ですよ。
洞窟探検って、サイエンスに通じるところがあるんですよ。特に、未踏の洞窟だと、人類が一度も光を当てたことがないところに自分がはじめて光を当てるわけです。それをやりたかったんです。
じゃ、ミクロの決死圏で肺の中に入ったらバッチリですね。
そうそう、3Dのイメージングとかまさにその状態ですよ。
サイエンスは命の危険はないと思うんですけど、洞窟探検って帰れなくなりそうで……。
帰ってこれますよ。大丈夫です。
だれも行ったこともない、ということは地図とかないでしょ?
探検と言っても、ちゃんと計画して、装備を持っていくから大丈夫。これは実験も同じですね。失敗してもいいからやってみろ、というのは半分ホントで半分ウソだと思っています。
というのは、予想してちゃんと計画して、準備して、それでも失敗したら得るものがあるけど、計画も準備もしていないでとりあえずやってみた、で失敗、は無意味です。

なので、本当の意味で「失敗する実験」はやっちゃダメだと思います。研究費が少ないときによい成果が出たという研究者の成功談はよく聞きますよね。お金がないと無駄ができないから、考えて・考えて・考えて・考えてやるから結果が出るんだと思うんです。
なるほど。結構思いつきでやりっぱなしのこと多いですからね。反省します……。
編集後記
ぱっと見優しそうな雰囲気の森本さん。でも、洞窟探検をしたりかなりアクティブな方。研究の話をし始めたら止まらない、止められない……。本当に生物が好きなんだなー。しかも基礎の部分を着実に積み上げている、というのがとてもよく分かるお話でした。再生医療は期待されているけれど、こういった基礎の積み上げの上に成り立っているんだな、と感服しました。
ちなみに、この記事ではインタビューということで細かいところは割愛しているので、森本さんの研究紹介ウェブサイトやギャラリーも併せてご覧いただくとわかりやすいです。
