生化学反応の基礎と応用
今回のゲストは鉄の研究者中村さんから横浜つながりで美川さん。BDRの拠点はいくつかあるけれど、神戸と横浜は分野が異なっていて、趣が違うので、たまの横浜の人インタビューが結構楽しみ。さてさて、今日はどんなお話になるのやら……。(聞き手:薬師寺秀樹)
いきなり液-液相分離
所属は細胞構造生物学研究チームということですが、研究の内容は構造生物学ってことになるんですか?
いや、ちょっと違うんですよ。
今やりたいことはタンパク質の動きを研究することですね。ラボの名前に構造生物学ってついているんですが、構造そのものというよりは、タンパク質の動きを研究して、タンパク質がどのように機能しているかを知りたいということですね。
特に、液-液相分離2つの液体が混ざり合わずに分離する現象。例えばドレッシングの中で水と油が分離するようなこと。といわれる、ここ10年くらいNature誌やScience誌をすごく賑わせている現象があるんです。日本でも近年ホットなトピックになってきています。
細胞の中でも、液-液相分離によって必要なタンパク質とかが集まってきて、今まででは考えられないような効率で反応を進める場みたいなのを作っていることが分かってきたんです。ラボでは、この液-液相分離とそれによってタンパク質がどのような影響を受けるのかを研究をしています。
でも僕はもともとは組換えの研究ををやっていたんです。
発生のときと修復のときは同じ仕組み
遺伝子組換えの意味の組換えですか?
そうです。組換えっていうのは、例えばDNAのどこかが傷ついたりした時に、そのまま放っておくとその細胞が死んじゃったりがんになったりするので、その傷ついた部分を直すような時にも働くんです。僕はその組換えの時に働くタンパク質をNMRなどを用いて構造生物学的に解析していたんです。
DNAを修復するときって、たぶん損傷部位を発見するとか、必要なパーツを呼んでくる、あるいは実際に直すとか、いろいろ機能を持ったタンパク質が関わると思うのですが、どれを狙ってたんですか?
僕がメインでやっていたのはDNAを組換える役割を持ったタンパク質ですね。DNAの似た配列を見つけてきて、そこをコピー・アンド・ペーストするようなシステムがあるんです。僕らは父方と母方の遺伝子を1個ずつ持っているんですけど、例えばどっちかが完全にすっ飛んでしまったときも、それをもう1組の方からコピーして直すことができるんです。組換え修復というものなんですけど、そこに働くタンパク質の構造機能解析というのをやっていたんです。
へー。面白い。その組換えをするタンパク質って、何をするんですか?
DNA修復にも効いているんですけど、ヒトなど高等な生物だと、遺伝でも重要な働きをしています。例えば、精子とか卵をつくる減数分裂という過程で、父方と母方由来の遺伝子を混ぜ合わせるんです。例えば、僕みたいに、男の人だったら精子を作りますよね。その場合に、父親方だけの遺伝子が入った精子と、母親方の遺伝子の入った精子ができるわけじゃなくて、必ず父親と母親の遺伝子を混ぜ合わせた精子を作るんです。そのタンパク質が、DNAの傷を直すのにも使われているんです。
そのタンパク質は具体的に何をやるんですか? コピー・アンド・ペースト?
DNAにフィラメントをつくるんです。
また出た、新しい単語。フィラメント。
タンパク質ってよく1個だけで働いているところをイメージしがちなんですけど、そうではなくて、DNAの上にもう何百個とずっとつながってDNA上にタンパク質-DNAフィラメントというものを作るんです。そして、そのフィラメントと同じ配列のDNAをものすごい効率で探し出して、そこと組換えるという、そういう働きをするタンパク質があるんです。
ちなみにそのDNAに傷がついた場所というのは、サイズはあまり問わないんですか?
問いません。1塩基だけが飛んだだけじゃなくて、ざっくりと抜けてしまったとかでも大丈夫ですし、減数分裂のときは別に損傷してなくても似たようなところで入れ替えます。だから、損傷で使われるタンパク質と、減数分裂で使われるタンパク質が基本的に同じということですね。
それは面白いですよね。傷が入ったときに直すやつと、生まれるときが同じものでできてるということですよね。
同じものを使っていますね。似たような場所を探して、そこの部分を対になるDNAからコピーして入れ替えたら組換えになるし、失った部分をコピーして戻したら修復になるという感じ。
結晶構造だけじゃわからない
今素朴な疑問が湧いたんですけど、対になる同じ配列が3次元空間上で近くにあるとは限らないじゃないですか。
そうです。そこがすごく不思議なところなんです。しかも、何十億という塩基対の中から、正確にその場所を探し出すんです。ここにも液-液相分離が関与していると思います。液-液相分離で離れたDNAが組換えを行うタンパク質と集まって反応の場を作るんです。結果、その中で実際にDNAが組換えられるわけですが、その反応メカニズムを調べるのが結晶構造解析だと難しい。
タンパク質の構造解析とか構造機能解析というのは、小さくて溶液中によく溶ければNMRで、結晶ができればX線結晶解析とかできるんですけど、フィラメントみたいに束になっていたりすると、解析が非常に難しくなって、いまだにこのDNAをフィラメントの中でどうやって組換えているのかというのは、結局まったくわかっていないんです。
それは結晶化が難しい?
結晶化はされているんですけど、結晶の中で固まった形を見ても、どうやってDNAが組換わっているかは分からないということです。DNAが中に入った結晶構造も解かれているんですけど、それでも分からないんです。
なんでわからないんですか?
それはやっぱり反応前と反応後の絵しかないので、結局組換わる前にくっついているところと、組換わった後にくっついているところの写真が取れているだけで、反応中のブラックボックスのところの写真がまったく取れていないんです。
ビフォーとアフターしか分からない。
分からないですね。そのブラックボックスのところはたぶん非常に一瞬に起こってしまって、結晶とかでは捉えられないんです。でも、DNAが切れたところにタンパク質が集まって来る時に、液-液相分離が起こっているんじゃないかということが分かってきたんです。DNAが切れた場所というのは、その切れた場所に切れたよというサインになるようなものを作るんです。そうすると、そこを起点にタンパク質が寄ってきて、そこがわーっと相分離するんです。そうすると、液―液相分離したところにいろいろな因子が集まってきて、修復がきれいに完了するとか、そういう話になってきています。
想像を超えていて、イメージが追いつかないですね。
そうですね。ちょっと本当にまだ最近と言ったらあれですけど、そんなに教科書とかにもちろん載っていないような話なので、まだ。そういうイメージになっちゃいますかね。
いろんなところに液-液相分離
液-液相分離って、単語としては聞いたことがあるし、相分離が液相と液相で起こるんだろうなというところまでは日本語としてはわかるんですけど、例えば細胞の中で液-液相分離というと、具体的なイメージとしてどんな感じなんですか?
顕微鏡下では普通に玉に見えるドロップレットという、日本語でいうと液滴ですね、そんな風に見えます。溶液の中で玉に見えて、それが融合したり、分離したりもします。細胞の中っていろいろな区画がありますよね。核があったり、ミトコンドリアがあったりという感じで。ドロップレットは膜のないオルガネラというイメージです。液-液相分離によってポコンとドロップレットになったところはいろいろな反応を起こしやすい場になるんです。そういった現象で、多くの生命現象が効率良く起こることが説明できるようになってきたのがここ10年くらいです。
その玉はどうやって、できてくるんですか?
タンパク質って構造を取っていない、つまりフラフラしている部分をいっぱい持っているんです。intrinsically disordered region、IDRとか、天然変性領域というものです。
構造のある部分はX線結晶解析で結晶をつくって構造を解くんですが、結晶の構造のないところは、そもそも結晶にはならないから、みんな切って捨てていたんです。そんな構造がない部分をタンパク質がいっぱい持ってるのはなぜだろうという謎は置いておかれてたんですけど、実は構造のない部分というのが、この液-液相分離を起こすということがわかってきたんです。この構造のない部分が、ある環境になると、そこ同士がぐっと集まってきて、液滴をつくったりするんです。
細胞の中は均質じゃない
そうすると細胞の中の液体の成分が均質じゃないということが起こるんですか? なんとなく均質なもののイメージになっちゃうんですけど。
いや、細胞の中は全然均質じゃないですね。どっちかというと右のほうと左のほうじゃ全然違うものがあるという感じですね。液-液相分離というのは、そういう中でもなんかの環境になったときに天然変性領域とか核酸なんかを起点にして、がーっとみんなが集まってきて、ポンとそういう場を作っちゃうんです。なので、そのときだけできるオルガネラみたいな感じになるんです。
ある程度用が済んだらというか、やることをやったらまたふわーっと解散していくんですか、これまた。
そうです。今まで液-液相分離という概念がないときから、こういった物質はあって、例えばストレスグラニュールとかって聞いたことありますか?
ストレスがたまると出てくるやつですか?
そうです。ストレスグラニュールというのは、細胞を飢餓にしたりとか、ストレス状態にすると、なんかやっぱり細胞の中に玉みたいなのができるんですよ。

結局これも、RNA結合タンパク質とRNAが集まって、液滴というものをつくっていたんです。これが何をしているかというとメッセンジャーRNAを守ったり、壊したり、翻訳をちょっと待ってもらったり、必要なときまで保護したりとか、飢餓状態のときに働くと良くないものを、ちょっとエスケープ的に溜めている感じなんです。それも、今まではそういう物質があるというのは分かっていたけど、それが液-液相分離で起こっているとは分かっていなかったんです。
グラニュールだから、玉ができるよということは分かっていたってことですか?
分かっていたんですね。でもこれが溶液状だとは誰も思っていなかったんです。オルガネラではないんだけど、そういった玉が細胞の中にはたまにできる、みたいな感じだったんですけど、これは実際、RNA結合タンパク質というのがさっき言った天然変性領域を持っていて、それとRNAが結合するとガーッと集まってきて玉になっていたんです。ある条件が整うと、その玉がほどけて、必要なメッセンジャーが翻訳されたりします。
すごい不思議ですね、これ。
こんなことが細胞の中でとにかくいっぱい起こっているということがわかってきたのが、本当にここ10年くらいなんです。
これ、どうやって特定するんですか?
例えば、ストレスグラニュールだと、ストレスグラニュール自体を取ってくることはできるんです。
液-液なのに?
液-液なんですけど、意外と細胞をつぶしても安定に玉のままいるんです。
これまた不思議ですね。
液-液相分離なので、そうなることが安定なのでそうなっているんです。その状態が安定だからその玉になっているので、細胞をつぶしても玉で残っているわけです。なので、その玉だけひょいと取ってきて、その玉に何が含まれているかというのをわーっと調べることができるんです。
今までの酵素活性は間違っているかも……?
液-液ってそういうことなのか。何が安定に寄与しているんですかね。密度?
液-液相分離でできるドロップレットもいろいろな種類があるんです。例えばつぶす方法で分類したりもできます。塩濃度をすごく上げるとつぶれるものだと、静電的相互作用が重要なんだろうという話になる。アルコールみたいなものでつぶれるんだったら、疎水性の相互作用が重要なのかなとか。なので、どれも同じもので壊れるわけではないので、全部同じ仕組みでできているわけではないんです。
めちゃ不思議。
さらにもっと面白いことがあって、液-液相分離でできたドロップレットの中にある酵素の反応効率が高くなることがあるんです。例えば、溶液中の反応効率が1しかないとしますよね。だけど、ドロップレットの中だと100とか出たりするんです。
それ、ちょっとえらいことですよね。今まで酵素の活性度って試験管とかで測るけれど、実際の活性度って全然そんなもんじゃなかった、みたいな話になっちゃいますよね。
そうなんですよ。それが面白いので、今はドロップレット内にある酵素の機能解析を中心に行っています。
そんな大きなフィールドになりつつあるんですね、液-液相分離って。
工業的にも広がると思いますね、うまくいけば。連続反応ってあるじゃないですか。例えば我々だと代謝系というのがあって、糖を食べたら、それがどんどん分解されていくんだけど、その中に酵素が何種類もあるわけですよね。AをBにする酵素、BをCにする酵素って。それで大体3段階も進むと、シミュレーションではもう分散して反応が進まないはずなんです。でも、細胞の中って、きれいに最後まで進むんです。
それもものすごい不思議ですよね。
それも相分離で説明がつくんです。これらの酵素群がドロップレットとしてまとまれば、連続反応の効率はものすごく上がります。少なくとも酵素はかなり工業で使われているので、今後もっとフィールドが広がっていくと思います。
そしてバイオ燃料電池

それで、バイオ燃料電池の研究もやってるんです。
なんかあると思っていました(笑)。
バイオ燃料電池というのは、酵素で発電するんですけど。アルコールを作らせて、それを使うというわけではなく、直接発電します。
ちょっと解説をお願いしてもいいですか。
ブドウ糖でも油でも有機物であればなんでもいいんですが、酸化されると、電子が引き抜かれます。一方で反対側は還元酵素を置いておきます。この還元酵素がさっき取ってきたこの電子で酸素を還元して水にするんです。つまり、有機物を燃焼して、有機物を酸化しながら発電をするというシステムなんです。
酸化する酵素と還元する酵素という感じですかね、イメージとしては。
これは燃料電池なので、それを下敷きにしたら分かりやすいかもしれません。燃料電池だと、水素が白金触媒で分解されて、水素イオンになって、水素と水素の中にある電子が取り出されて、それが反対の白金極で酸素を還元して水が出てくるという形になります。そのいわゆる燃料電池の白金触媒の代わりに酵素を触媒に使って、水素の代わりに糖などの有機物を燃料にしているというわけです。なので、あらゆる有機物を燃料にその有機物を酸化する酵素のペアで電池にできるということです。
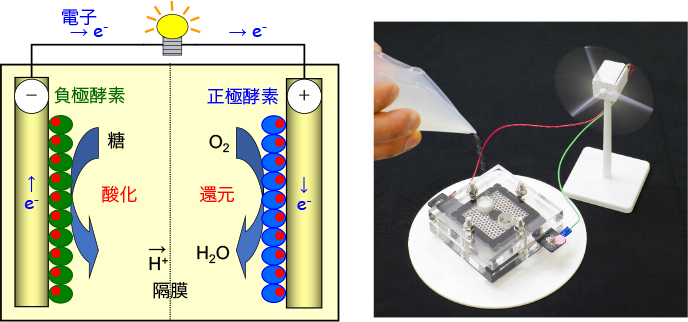
例えば、燃料がグルコースだとすると、グルコース酸化酵素を電極に乗っければいいんです。
ペアが作れればなんでもいいんだ。
はい。今僕らが作っているのは、乳酸ですね。乳酸を酸化する酵素、乳酸酸化酵素で作っています。そうすると、汗に含まれる乳酸で発電するので。
原料ゼロ円ですね。
出てきた汗で発電して、それで体調をモニタリングして、そのデータをスマホに飛ばすみたいなこともできます。
使い道いろいろありそうですね、これ。
今はとりあえず汗から発電ということを目指しているんですけど。
でも、コストという意味では、いまある燃料電池なんかの出力って、いわゆる普通のコイン電池とかと同じくらいなんです。だからこのままではコイン電池に取って代わらないんです。
わざわざここまでしなくても普通の電池でいいじゃんということですか。
はい。でも、生化学の反応はエネルギーを使い切るまでに何ステップもありますが、今は1ステップ分しか実現できていません。だから今はまだ既存の電池に負けるんです。2段階分くらい使えるようになるとリチウムイオン電池くらいになりますが、これでまだ今よく使われている電池並みです。だけど3段階分、4段階分と使えるようになると、今世の中にある電池以上の電池になります。だから、4段階、5段階、6段階とかいくような電池を実現したら、スマホとかはたぶん1週間充電しなくてもお砂糖で動くようになると思います。
スマホが一週間も砂糖で動く!おもしろいですね。充電がいらなくなるってことですよね?
はい。燃料電池なので、燃料を足せばいいんです。そういうことを実現したくて、そのためには生体内並みの酵素の多段階反応を実現しないといけなくて、酵素の多段階反応を実現するためには、液滴が何をやっているか分からないといけなくて。というふうに登ってきて、最初の液-液相分離の話につながるんです。
壮大な話だ。ようやくつながりました。
さまざまな応用への期待
このバイオ燃料電池は汗で動くバージョンとか、いろいろあるんですよ。一般公開とかだと、よくやるのが、砂糖の入った炭酸飲料とシュガーフリーの同じブランドの炭酸飲料を子どもに選んでもらって、お砂糖が入っている方は酵素が反応して発電するんですけど、シュガーフリーのほうは類似物だけど分解できず、発電しない、とか。
人工甘味料系では動かないと。
動かないですね。
理研の中でも、こういうことを研究している人は何人かいいて、たまに集まって議論したりしています。
今乳酸で体調モニタリングにも取り組んでいます。僕らの作った乳酸の発電を使って、体温を測ったり、熱中症予防とか、汗の量を測ったりとか、そういったことをできないかというテーマです。
勝手に妄想を広げたくなりますね、これ。
さっきの電池の話で、7段階まで反応を組めたら今までにないものを作ることになるので、たぶん一気に加速すると思うんですけど、そのために、やっぱりどっちかというと基礎のほうでそれを実現しないといけないので、なかなか大変です。
人為的にドロップレットを作ってやって、その中に7ステップの反応を仕込んでやってということができたら、できちゃうかもしれない。
化けると思って信じてやっているんですけどね。
それ見てみたいですね。
そこまでいかないと、やっぱり意味のあるものにはならないですね。面白いだけのもので終わると思います。
けっこう工学的な考え方をされているんですね。
組換えの研究をしている時も発想としてあったのは、せっかく組換えのことをすごい勉強したので、その組換えを使って、試験管内で進化を実現させたいと思ったんです。要は分子進化の方法として、生命が使っているシステムをそのまま使うというイメージです。試験管の中に生命が行っている組換え反応を再構築して、遺伝子をどかっと入れる。その遺伝子をごちゃごちゃ混ぜていると、新しい遺伝子を創ってくれるというような。意味のないぐちゃぐちゃなものもできるけれど、中には新しい機能を持ったタンパク質ができるかもしれない。そうやって生命は進化してきたはずなので。要は、組換えを使って、まだ世の中にはない機能を持った酵素を作れないかという発想なんです。それもやりたいことの一つですね。
組換えにしても、きっとDNAとして気持ちがいいというか、スムーズに反応が進むポイントというのがあるんでしょうね。
たぶんDNA上にそういったものも記憶されているんだと思います。それは学問としてはまだないわけですが、DNAって塩基の数だけで言えば4種類しかなくても、数塩基つながればすごいバリエーションになっていくわけで、そうすると、やっぱり組換えが起こりやすい場所というか、組換えを許容されてきた場所と、組換えが許容されてこなかった場所とか、たぶんそういった情報は残っているんじゃないかなとは思います。
DNAは配列ですけど、最終的には構造になりますよね。それを組換えるタンパク質が見つけやすい場所とかが、僕らは配列しか見ていなくて想像もつかないけど、彼らからすると、ここはOK、ここは駄目だとかっていうのが分かって、いいところで組換えたり、悪いところでは組換えなかったりするのかなというイメージがあるんです。
ありそうですね。どうしてもDNAとか核酸、RNAとかって、シーケンスのイメージが強いので、配列情報として認識しがちですけど、実際たぶん細胞の中で見ていたら構造物ですもんね。
そうですね。なので、おそらくそういった情報はあって、それをうまく使っているのかもしれないですね。
幅広いですね、お仕事が。
基本的には基礎をやっていて、結局ものにしないともったいないという感じですかね。
例えば試験管の中でDNAを組換えられるようになったということはそれなりにすごいことなんですけど、組換えの業界ではよくやったと言われるかもしれないけど、世の中全体からしたら、あまりインパクトのある話ではないかもしれない。とはいえ、基礎の部分をきちんと実証していくという積み上げの部分が大事なんですよ。特に新しい分野ですからね。

編集後記
基礎研究っていろんな所に繋がるというのは頭ではわかっているけど、まさか遺伝子組み換えがバイオ燃料電池まで繋がるとは思わなかった。グルコースのエネルギー効率は高いことは言われているけれど、使い切るには7段階くらいの反応が必要でそれをやるには液-液相分離という新しい概念が必要で……。こういう積み重ねでいろんなことができていくんだなぁ。
