2021-03-26
最近の研究成果(2020年12月〜2021年2月)
2020年12月から2021年2月までのプレスリリースと論文ニュースからご紹介します。
ホルミシス効果の獲得と継承を担う小分子RNA
2021年2月17日
生物は常にさまざまな環境ストレスにさらされています。過度なストレスは生物に悪影響を与えますが、マイルドなストレスを経験した個体はしばしばストレス耐性を獲得することが知られており、これは「ホルミシス効果」と呼ばれます。驚くべきことに線虫では、親の世代で獲得されたホルミシス効果が数世代にわたって子孫にも継承されることが観察されています。岡部恵美子リサーチアソシエイト、宇野雅晴研究員、西田栄介チームリーダー(老化分子生物学研究チーム)らはストレス刺激で生成される小分子RNAに注目し、酸化ストレス耐性の獲得と継承に果たす役割を解析しました。その結果、ストレス刺激により神経、腸で生成されたある種の小分子RNAが生殖腺に運ばれ別の種類の小分子RNAなどを介して次世代へ伝える記憶を形成することで、親から子孫へとストレス耐性が受け継がれることが明らかになりました。 続きを読む
Okabe E, Uno M, Kishimoto S, Nishida E. Commun Biol 4, 207 (2021)
環状ペプチドは立体構造を変えて細胞に入る
2021年2月16日
環状ペプチドなどの中分子薬剤は、細胞の中で起こるタンパク質とタンパク質の相互作用を阻害する新しいタイプの薬剤として注目されています。しかし、環状ペプチドが薬として効果を発揮するためには、まず、細胞の膜を透過して、細胞の中へ入る必要があります。そのため、中分子医薬の発展には、細胞内への移行性を高める論理的なデザインが求められています。嶋田一夫チームリーダー(生体分子動的構造研究チーム)らは、化学的性質が類似しているにもかかわらず細胞内への移行性が大きく異なる環状ペプチド群について、立体構造を核磁気共鳴法を用いて比較しました。その結果、両者は水溶液中では同様の立体構造を示しますが、細胞膜を模倣する有機溶媒中では、細胞内へ移行できる環状ペプチドは両親媒性(水と油の両方になじむ性質)構造を形成するのに対し、細胞内へ移行できないペプチドは、隣り合うアミノ酸の側鎖同士の立体的な障害により、両親媒性構造を形成できないことが分かりました。このことは、溶媒環境に応じた柔軟な構造変化が、環状ペプチドの細胞内移行を左右する重要な要素であることを示しています。 続きを読む
Takeuchi K, Misaki I, Tokunaga Y, et al. Angew Chem Int Ed Engl (2021)
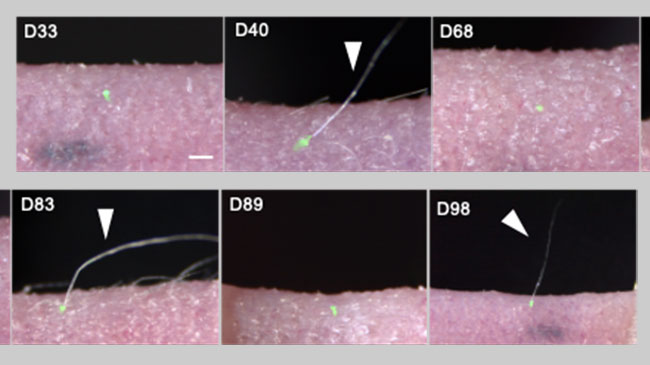
周期的な毛包再生を可能とする上皮性幹細胞の増幅と特定
2021年2月10日
哺乳類の毛髪の成長は、毛が成長し、抜け落ち、再び生えてくるという周期的なプロセスです。毛包には、複数種の上皮性幹細胞が存在しますが、長期間の周期的な毛包再生を可能とする細胞集団の実体は長らく不明なままで、その生体外増幅法も確立されていませんでした。辻孝チームリーダー、武尾真上級研究員(器官誘導研究チーム)らは、幹細胞を用いて失われた毛髪を再生する方法に取り組んできましたが、 今回、毛包再生能力を維持したまま毛包幹細胞を生体外で100倍以上増幅する培養方法を確立し、さらに長期間にわたる周期的な毛包再生に必要な幹細胞集団を明らかにしました。 続きを読む
Takeo M, Asakawa K, Toyoshima KE, et al. Sci Rep 11, 1173 (2021)
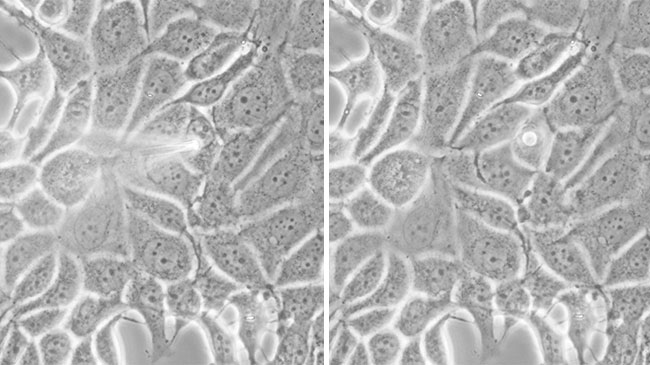
がん細胞1個から中分子薬剤の細胞膜透過性を評価
2021年2月6日
分子量が500~2000程度の環状ペプチドは中分子薬剤と呼ばれ、通常の低分子の薬物と同様に細胞内へ浸透させることが可能です。また抗体医薬品のように特定の分子に結合することができることから、細胞内部の病変分子を標的とする次世代治療プラットフォームとして期待されています。しかし、環状ペプチドの細胞内への浸透性を評価する手法は存在していませんでした。川井隆之研究員(一細胞質量分析研究チーム)、渡邉朋信チームリーダー(先端バイオイメージング研究チーム)らは、乳がん細胞をシクロスポリンAなどの環状ペプチドとともに培養した後、マイクロニードルを用いて細胞1個から細胞質のみを吸い取り、そこに含まれる環状ペプチドを高感度に計測する「一細胞細胞質質量分析法」を開発しました。この技術を用いて、これまで解析が難しかった細胞質中の薬剤濃度の時間変化を追跡し、環状ペプチドの細胞膜透過性と細胞内濃度を同時に評価することに成功しました。 続きを読む
Kawai T, Mihara Y, Morita M, et al. Anal Chem 93, 3370-3377 (2021)
細胞のリプログラミングを追う光技術
2020年12月25日
分化した細胞を未分化な状態に初期化すること(リプログラミング)によって作製される人工多能性幹細胞(またはiPS細胞)は、成体のすべての種類の細胞を作り出す能力を持っており、再生医療の要として有望視されています。リプログラミング中の細胞の変化を解析するために、アルノ・ジェルモン研究員、渡邉朋信チームリーダー(先端バイオイメージング研究チーム)らは、ラマン分光法として知られている分析技術を用いました(トップ画像)。ラマン分光法はレーザービームを用いて分子に固有の波長の散乱を測定するため、既存の方法に比べて侵襲性が低く、迅速に、かつ低コストで行うことができます。研究チームは、ラマン分光法で得られるスペクトルがリプログラミングの進行を示すバイオマーカーとして利用できることを示しました。 続きを読む
Germond A, Panina Y, Shiga M, et al. Anal Chem 92, 14915-14923 (2020)
翻訳阻害抗がん剤の二つ目の標的を同定
2020年12月10日
DNAの遺伝情報はmRNAに転写され、さらにリボソームでタンパク質に翻訳されます。これまで、転写が遺伝子発現を決めていると思われていましたが、近年、翻訳の過程でも、調節が起こっていることがわかってきています。ガンの抑制剤の一種であるロカグラミドA(RocA)は翻訳開始因子であるeIF4Aに結合し、翻訳を阻害し、がん細胞の増殖を抑制することがこれまでの研究で分かっています。今回、理研開拓研究本部の岩崎信太郎主任研究員、袖岡幹子主任研究員、BDRの伊藤拓宏チームリーダー(翻訳構造解析研究チーム)らの共同研究グループはロカグラミドAが標的とするタンパク質として同じく翻訳開始因子の一つであるDDX3を新たに同定しました。またロカグラミドAの細胞増殖抑制効果はDDX3およびeIF4Aの発現量が多いがん細胞ほど高いことを明らかにしました。今後は、事前にがん細胞が発現するこれらの標的タンパク質量を調べることにより、ロカグラミドAが効きやすいかどうかを診断できるようになると期待できます。 続きを読む
Chen M, Asanuma M, Takahashi M, et al. Cell Chem Biol (2020)

シビレエイを用いた海底地形探査
2020年12月8日
海底には豊富な天然資源があり、それを利用するためには海底地形地図の作成が必要です。現在はロボット、ソナー、あるいは人工衛星などを用いた方法によって地図が作成されています。田中陽チームリーダー(集積バイオデバイス研究チーム)らはシビレエイの自然な泳ぎ方を利用した全く別のシステムによる地図作成を提唱し、海洋探査実験を行い、その可能性を検証しました。まず、実験施設内のプールで底棲生物であるシビレエイがほとんどの時間、底付近を動いていることを確認しました。次に、シビレエイに小型音響送信機ピンガーを装着して海底に放ち、ピンガーからの信号を船に取り付けた複数の受信機で受信することで、その信号の到達時間差から位置を計算しました。その結果、シビレエイの位置から水深情報を取得し、海底の地形情報を得ることができることを実証しました。 続きを読む
Funano S, Tanaka N, Amaya S, et al. SN Applied Sciences 2, 2142 (2020)

ヒューマノイドロボットとAIによる自律細胞培養
2020年12月4日
再生医療で使用する高品質な細胞を効率的に生産することは、再生医療の重要なステップですが、現状では多くの場合、細胞の培養・製造は熟練技術者による匠の技に依存しています。今後、再生医療の標準化と普及をめざすためにはプロセスの機械化や自動化により、人間の介入を減らしていく必要があります。髙橋恒一チームリーダー、落合幸治大学院生リサーチ・アソシエイト(バイオコンピューティング研究チーム)、許沢尚弘大学院生リサーチ・アソシエイト(網膜再生医療研究開発プロジェクト)らは、ヒューマノイドロボットと人工知能を組み合わせることによって、人間の手と頭を介さない自律細胞培養システムを開発しました。この成果は、生物学実験の自動化による研究効率の向上、手法の標準化ならびに、遠隔実験・自動実験が要請されるコロナ時代の新研究スタイルの確立につながるものとして期待できます。 続きを読む
Ochiai K, Motozawa N, Terada M, et al. SLAS Technol (2020)
